
РЕАКТИВЫ
1. Раствор трилона Б. 0,05 н. раствор трилона Б получают в результате растворения 9,3 г трилона В в дистиллированной воде с последующим доведением объема до 1 л в мерной колбе.
2. Буферный раствор 20 г химически чистой NH4C1 растворяют в дистиллированной воде, добавляют 100 мл 20%-ного раствора NH4OH и доводят дистиллированной водой до 1 л.
3. Раствор индикатора 0,5 г эриохрома черного Т растворяют в 10 мл буферного раствора и доводят до 100 мл этиловым спиртом (96%-ным).
Пользуясь указанной выше формулой, В. П. Дацкевич составил таблицу, дающую возможность без сложных расчетов получать результаты титрования в градусах жесткости. В табл. 4 нужно найти цифру, равную количеству миллилитров трилона Б, пошедших на титрование. В левой (вертикальной) графе находятся градусы жесткости, в верхней (горизонтальной) - десятые части градуса.
Таблица составлена для анализа, проводимого в 100 мл воды 0,1 н. раствора трилона В, либо 0,5 н. раствора трилона В, но при 50 м-л воды.
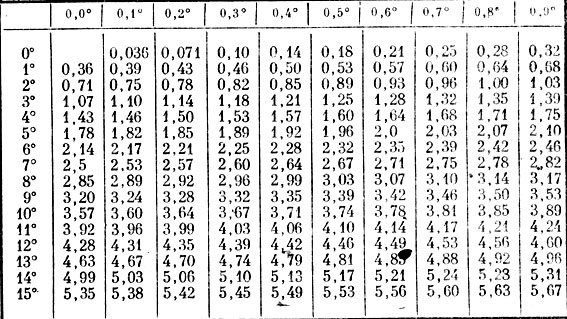
Таблица 4. Определение жесткости воды по расходу трилона Б
Для содержания и особенно разведения многих рыб водопроводная вода ряда городов Советского Союза недостаточно мягка и ее приходится в значительной степени смягчать. Основным методом смягчения воды является смешивание ее к определенных пропорциях с дистиллированной или дождевой водой. К сожалению, дождевой водой, как и водой из талого снега, в крупных промышленных центрах из-за загрязненности воздуха пользоваться нельзя. Только после 2 - 4-часового непрерывного выпадения атмосферных осадков воду можно использовать, да и то после фильтрования и длительного отстаивания. Известно несколько способов смягчения воды.
Первый способ основан на удалении устранимой жесткости. В результате кипячения в течение часа в большинстве случаев жесткость воды снижается вдвое. Для кипячения лучше употреблять эмалированную или стеклянную посуду. После охлаждения на воздухе или в холодной воде осторожно сливают 1/3 содержимого сосуда, остатки с выпавшим осадком выплескивают. Образовавшаяся со временем накипь удаляется со стенок сосуда слабым раствором соляной кислоты.
Второй способ более сложен, он требует определенного оборудования. Проще всего приобрести в магазине лабораторного оборудования готовый дистиллятор любого гипа, но лучше газовый или электрический. Такие дистилляторы дают до 4 л/час. В случае отсутствия фабричного дистиллятор легко изготовить самим, используя 3 - 5-литровую колбу и водяной холодильник, который можно заменить двумя стеклянными трубками разного диаметра, но желательно большой длины (70 - 100 см). Такие дистилляторы дают воды до 1,5 л/час. Вода, полученная этим способом, имеет жесткость до 1 - 2°. Дистиллированную воду можно приобрести и в аптеке.
Третий способ наиболее эффективен и экономичен. Он осуществляется химическим обессоливанием с помощью ионитов.
Соли, кислоты и щелочи в воде находятся в виде ионов: катионов и анионов. Например, поваренная соль NaCl в виде катиона натрия Na+ и аниона хлора Сl- (плюс - знак катиона, минус - знак аниона).
Некоторые вещества, встречающиеся в природе, но в основном синтезированные искусственно, обладают способностью удерживать на своей поверхности различные ионы и при известных условиях обменивать их с большой скоростью на другие ионы, содержащиеся в растворе. Такие вещества называют ионитами или ионообменниками, чаще ионообменными смолами (обычно неправильно). Иониты, способные к обмену катионов, именуются катионитами; иониты, способные к обмену анионов, анионитами.
В нашей стране выпускается большое количество различных ионитов. В аквариумной практике из катионитов проверены КУ-1 и КУ-2, из анионитов - эспатит АН-1 к ЭДЭ-10. Пропуская водопроводную воду последовательно через катионит и анионит, можно получить практически обессоленную воду, не уступающую дважды дистиллированной воде.
Процесс обессоливания при помощи ионитов проходит следующим образом. Установка состоит из двух стеклянных цилиндров длиной 50 - 60 см и диаметром 40 - 50 мм, укрепленных на штативе (рис. 66). Каждый цилиндр снабжен на концах резиновыми пробками со вставленными в них стеклянными трубками. Первый цилиндр (с катионитом) соединяется с одного конца резиновым шлангом с водопроводным краном, а с другого - с цилиндром, содержащим анионит, из цилиндра с анионитом течет обессоленная вода. Чтобы вместе с водой не попадали частицы ионита, на дно цилиндров кладутся либо стеклянная вата, либо стеклянные палочки, а затем стеклянная вата. И катионит, и анионит перед употреблением необходимо залить водой в открытом сосуде и дать постоять в течение нескольких часов, так как иониты разбухают и могут разорвать цилиндры. После набухания катионит и анионит обрабатываются по-разному. Катионит обычно сразу же засыпают в цилиндр и через него пропускают 1,5 - 2 л раствора 5%-ной соляной кислоты в дистиллированной воде (в зависимости от количества катионита, помещенного в цилиндр, и его обменной емкости). Промыв катионит 2-3 л дистиллированной воды, его можно использовать.
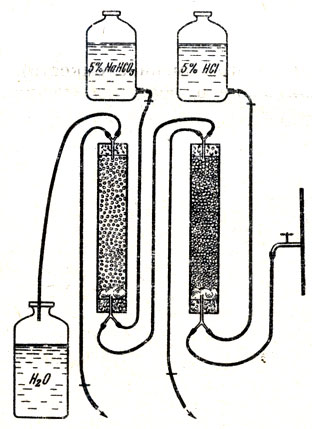
Рис. 66. Ионообменные колонки
Анионит требует более длительной обработки. Набухший анионит засыпают в цилиндр и через него пропускают 5%-ный раствор питьевой соды на дистиллированной воде из расчета 6 л на 1 кг сухого вещества, затем его промывают 8 - 10 л дистиллированной или обессоленной воды.
Катионит при прохождении через него водопроводной воды обменивает все катионы (Са+, Mg+, Na+ и др.) на катион водорода Н+; анионит - все анионы (SO4, Cl, СО2 и др.) на ион гидроксила ОН-. Ион Н+ из катионита соединяется с ионом ОН- из анионита и дает Н2О. Таким образом, последовательно пропуская водопроводную воду через катионит и анионит, мы получаем полностью обессоленную воду.
В аквариумной практике часто вместо полного обессоливания воды с помощью ионитов производят смягчение ее Na-катиони-рованием или Н-катионированием; и в том и в другом случаях употребляется только катионит.
При Na-катионировании катионит регенерируют не соляной кислотой, а поваренной солью. Соответственно все катионы замещаются Na+ ионом. Следует отметить, что рабочая емкость при Na-катионированша несколько выше. Н-катионироьание проводится так же, как и при полном химическом обессоливании.
Вода, смягченная Na- и Н-катионированием, пригодна для икрометания многих рыб. Желательно только более или менее длительное ее выстаивание (до 2 - 3 недель). Именно при употреблении такой воды впервые в Москве были разведены неоны и расборы. Однако в большинстве случаев при употреблении такой воды сразу же после появления личинок рыб ее приходится заменять аквариумной, гак как для содержания рыб эта вода непригодна. Дело в том, что при Н-катонировании в воде оказывается катион водорода, который соединяется с освободившимися анионами и образует целый ряд различных кислот, таких, как соляная, серная и др. При Na-катионировании катион Na+ соединяется с анионами и образует соли: поваренную NaCl, глауберову Na2S04 и др. При катионирования очень жесткой воды концентрация кислот или солей становится чрезмерно высокой. В таких случаях этот способ не может найти практического применения.
Дистиллированная или химически обессоленная вода служит для приготовления воды общего или нерестового аквариумов. Водопроводную воду следует подогреть в течение 30 - 40 мин при температуре 90° и затем охладить. Полученную воду смешивают в определенной пропорции с обессоленной с таким расчетом, чтобы получить воду необходимой жесткости. Пропорцию легко составить и сделать расчет, пользуясь приводимой табл. 5.
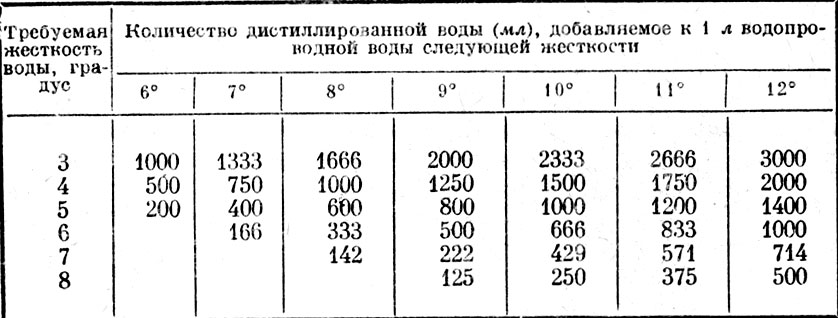
Таблица 5. Приготовление воды нужной жесткости
Например, жесткость водопроводной воды 9°, необходимо получить воду с жесткостью 5°. По горизонтали в таблице указана жесткость водопроводной воды, по вертикали - требуемая жесткость. В графе, находящейся под цифрой 9°, находим данные, соответствующие цифре 5 вертикального столбца. Из таблицы видно, что для получения нужной жесткости к 1 л водопроводной воды следует добавить 800 мл дистиллированной.
Таблица дает точные данные лишь в том случае, если мы пользуемся химически обессоленной водой или дважды дистиллированной, имеющей нулевую жесткость.
При пользовании дистиллированной водой необходимо вначало выяснить ее жесткость и при приготовлении воды ввести соответствующую поправку, а перед употреблением проверить жесткость полученной воды.
Для повышения жесткости воды в аквариумах иногда достаточно в грунт добавить кусочки известняка, мела, мрамора или старой известки. Можно повысить жесткость также кипячением воды, при этом после охлаждения и отстаивания кипяченой воды сливают 2/3 содержимого сосуда, а остаток выливают в аквариум.
В сосудах, лишенных рыб и растений, жесткость постепенно повышается за счет испарения воды и попадания пыли, еще больше может повышаться жесткость при наличии грунта, содержащего кальций. В действующем аквариуме калтций усваивается рыбами и другими животными (особенно моллюсками), а также растениями и используются на построение их тела.
Обычно добавление кальция с водой, наливаемой взамен испарившейся, а часто и его наличие в грунте не компенсируют снижения жесткости воды. Поэтому старая вода, как правило, бывает мягкой. Однако в зависимости от количества рыб, растений и других животных, от наличия кальция в грунте, а также от температуры, света и целого ряда других факторов наблюдаются различные, в том числе и суточные, изменения жесткости воды в аквариуме, включая и значительное повышение ее.
Активная реакция водородных ионов. Активная реакция водородных ионов (рH) имеет очень важное значение. Зависит она от концентрации водородных ионов. рН, равная 7,0, обозначает нейтральную среду, ниже 7,0 - кислую, от 7,0 до 14,0 - щелочную.
Водопроводная и большинство природных вод обычно имеют рН в пределах 6,5 - 8,5.
рН воды, во многом зависит от наличия свободной углекислоты: чем больше свободной углекислоты, тем вода кислее, при прочих равных условиях. В воде, лишенной солей, благодаря растворению угольного ангидрида (углекислого газа) реакция становится слабокислой. Например, в дистиллированной воде после непродолжительного стояния рН = 5,7. В отдельных случаях на величину рН оказывает влияние присутствие органических кислот, поэтому болотные воды часто имеют кислую реакцию.
Активная реакция водородных ионов не остается постоянной и подвержена сильным колебаниям как в течение года, так и в течение суток. Как правило, во всех случаях величина рН к утру сильно снижается ввиду накопления СО2, а вечером из-за потребления углекислоты растениями повышается.
Для всех водных организмов, включая и рыб, существуют определенные оптимальные условия концентрации водородных ионов.
В аквариумной практике принято считать: рН от 1 до 3 - сильнокислая вода, от 3 до 5 - кислая, от 5 до 6 - слабокислая, от 6 до 7 - очень слабокислая; рН 7 - нейтральная, от 7 до 8 - очень слабощелочная, от 8 до 9 - слабощелочная, от 8 до 10 - щелочная, от 10 до 14 - сильнощелочкая вода.
Кислая и сильнокислая, равно как щелочная и сильнощелочная вода для аквариумных рыб абсолютно непригодна. Слабокислая вода подходит для содержания и особенно разных видов икромечущих карпозубых. Нейтральная, очень слабокислая и очень слабощелочная вода подходит для содержания и размножения большинства видов аквариумных Большинство харацинид, хемиодонтиды, некоторые мелкие цихлиды, некотирьд у доборы предпочитают очень слабокислую и слабокислую воду, а для размноожения многих из них такая вода - необходимое условие. Очень слабощелочную воду предпочитают молинезии, дисковидный и бриллиантовый окуни.

Дисковидный окунь
Требования к условиям среды у рыб в течение жизниааого цикла меняются. Так, для периода их роста нужна вода с одним показателем кислотности, а в момент размножения - с другим. Все это требует от аквариумиста знания методов определения и регулирования кислотности воды.
Обычно водопроводная вода после кипячения имеет нейтральную реакцию. В качестве подкислителя (с одновременным смягчением) можно использовать отстоенную дистиллированную воду.
Если появляется потребность в более сильном подкислении воды, то можно использовать верховой торф, т. е. взятый из торфяников, расположенных на возвышенностях; мри кипячении его в дистиллированной воде рН понижается до 5,0. Обычно для этого необходимо небольшое количество торфа (2 - 5 г на 1 л воды). Кипячение производится в течение 10 - 30 мин до тех пор, пока вода приобретет коричневый цвет. После этого воду фильтруют 1 - 2 раза через воронку со смоченной предварительно ватой. Полученный фильтрат торфяного экстракта наливают в аквариумную воду в количестве, необходимом для придания ей янтарного цвета, а в воду нерестилища - до установления необходимой рН. Подкисление можно производить, добавляя фосфорную кислоту или танин, но эти методы часто приводят к гибели рыб и могут рекомедоваться лишь в крайних случаях.
В тех сравнительно очень редких случаях, когда появляется необходимость увеличить щелочность воды, можно воспользоваться питьевой содой. При этом в 200 г воды, взятой из аквариума, разводят питьевую соду до получения необходимой рН. Путем простого пересчета, исходя из объема воды, вычисляется количество соды, необходимой для установления нужной рН во всем аквариуме. Питьевая сода разлагается на щелочь и углекислоту.
В непродуваемых воздухом аквариумах подщелачивание производят утром или днем в период наиболее интенсивного фотосинтеза, при этом СО2, полнее усваивается растениями.
Электрометрический метод требует специальной установки и доступен лабораториям, поэтому обычно аквариумисты производят определенио рН колориметрически.
Колориметрический метод основан на свойствах некоторых органических красителей, называемых индикаторами, изменять свою окраску в зависимости от концентрации водородных ионов. Сам ход определения рН по цветной шкале Н. Н. Аля-мовского не представляет никаких трудностей и не занимает много времени. Определение рН значительно облегчается при употреблении готового прибора Алямовского, в котором цветная шкала представлена пробирками с раствором или стеклянными пластинками, на которых имеются цветные пленки.
Прибор Алямовского можно приобрести в магазине; если по какой-либо причине такая возможность отсутствует, то можно его изготовить самому.
Наиболее трудоемким процессом является приготовление цветной шкалы. Однако следует отметить, что шкала, как и индикатор, отличается большой стойкостью и при хранении в темном месте может служить несколько лет.
В пробирку наливают 5 мл исследуемой воды, прибавляют 0,1 мл универсального индикатора и после взбалтывания (не закрывая пробирки пальцем) подбирают в стандартной шкале пробирку, окраска жидкости в которой вполне соответствует цвету исследуемой воды в пробирке с индикатором.
Для правильного определения рН необходимо, чтобы диаметр пробирок стандартной шкалы и тех, в которых берется исследуемая вода, был одинаковым. Если вода в аквариуме имеет желтоватый оттенок, то перед определением рН от него необходимо избавиться. Для этой цели можно применить активированный уголь (угольные таблетки, карболен).
Приготовление универсального (комбинированного) индикатора. Универсальный индикатор получается путем смешивания двух индикаторов - метилового красного и бромтимолового синего:
а) 0,04 г сухого метилового красного растирают с 6 мл 0,01 п. раствора NaOH, смывают смесь дистиллированной водой в мерную колбу емкостью 100 ли, прибавляют 20 мл этилового спирта и доводят до метки дистиллированной водой;
б) 0,01 г бромтимолового синего растирают с 3,7 мл 00,01 н. раствора NaOH, смывают смесь дистиллированной водой в мерную колбу емкостью 50 мл, прибавляют 10 мл этилового спирта и доводят объем до метки дистиллированной водой;
в) оба раствора индикаторов сливают вместе.
В кислой среде смешанный индикатор дает красную окраску, в щелочной - синюю.
Приготовление цветной шкалы. Стандартная шкала для сравнения готовится из цветных солей - хлоридов кобальта, железа, меди и сульфата меди путем определенного сочетания их.кислых растворов.:
а) хлористый кобальт CoCl2 6H2O г (59,5 г в 1 л 1%-ный HCl)
б) хлорное железо FеСl3-6H2О (45,05 г в 1 л 1%-ной НСl);
в) хлорная медь СuСl2 2Н2О (400 г- в 1 л 1%-ной HCl);
г) сернокислая медь CuSО4 (200 г в 1 л 1%-ной НСl). Приготовив растворы солей, наливают их в стеклянные пробирки одинакового диаметра из бесцветного стекла согласно табл. В. Налив раствор, пробирки закрывают резиновыми пробками.
Определять рН воды можно и с помощью бумажных индикаторов, но при анализе воды из аквариумов эти индикаторы часто дают искаженные показатели.
Кислород. Для разных рыб в отдельные периоды их жизни требуется различное количество кислорода, растворенного в воде.
В воде, бедной кислородом, могут жить и нормально развиваться только рыбы, способные использовать для дыхания атмосферный воздух. К ним из рыб, содержащихся в аквариумах, относятся все лабиринтовые, панцирные сомики, вьюны и змееголовы.
Однако подавляющее большинство аквариумных рыб нуждаются в определенном количестве кислорода, растворенного в воде. Снижение количества кислорода ниже допустимых границ может привести к заболеванию и гибели рыб.
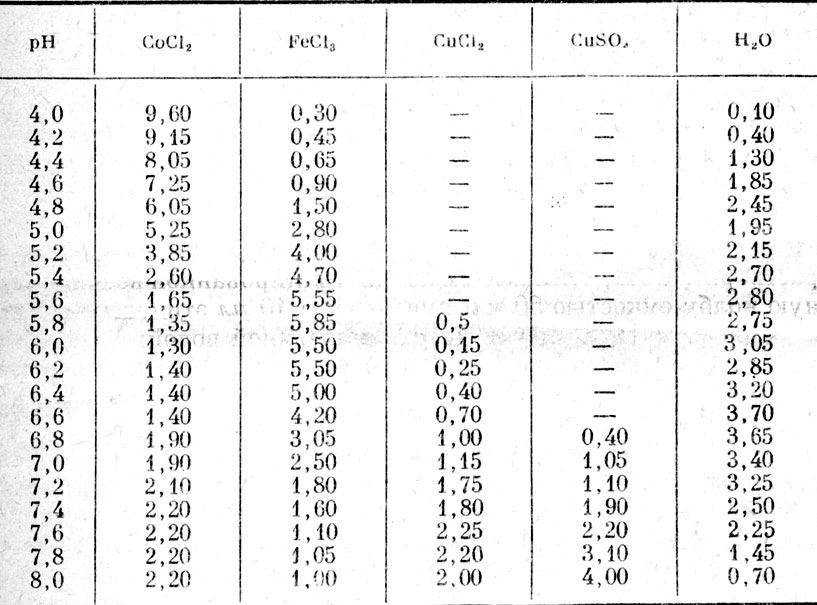
Таблица 6. Соотношение реактивов для стандартной цветной шкалы, мл
В аквариуме, предназначенном для выращивания молоди, может создаться такое положение, при котором рыбы будут вести себя обычно, однако рост их замедлится или прекратится совершенно. Падение содержания кислорода от оптимального до его дефицита вызывает снижение количества поедаемого корма, что, как правило, ведет к задержке или к остановке роста рыб, не говоря уже об опасности заболевания от недостатка кислорода. При подготовке рыб к нересту из-за недостатка кислорода может произойти задержка или прекращение созревания половых продуктов.
Источниками обогащения воды кислородом являются водные растения и атмосферный воздух. Скорость поступления кислорода из воздуха зависит от температуры воды. Кислород гораздо легче растворяется в холодной воде, чем в теплой, но, как правило, скорость его поступления бывает невысокой.
Мощным источником растворенного в воде кислорода является фотосинтетическая деятельность растений, в результате которой растения выделяют кислород. Интенсивность фотосинтеза зависит от содержания углекислоты в воде, температуры и освещения. Кислород, растворенный в воде, расходуется на дыхание животных и растений и па окисление органических веществ, растворенных и взвешенных в воде, а также осевших на дно. Количество потребляемого кислорода зависит от температуры.
Так как интенсивность фотосинтеза растений зависит от освещения, то в аквариумах без продувания воды воздухом наблюдаются резкие суточные колебания в содержании кислорода. В светлое время суток расход кислорода на окисление органических веществ и дыхание обычно перекрывается поступлением его в результате фотосинтеза. Ночью, когда фотосинтез прекращается, а потребление идет прежним темпом, содержание его начинает быстро уменьшаться, достигал минимума в предутренние часы. Естественно, что летом, когда ночь длится считанные часы, суточные колебания большого значения не имеют. Иное дело зимой, когда продолжительность дня равна всего лишь 7-8 час и количество кислорода в предутренние часы резко снижается.
Количество кислорода в воде аквариума может быть увеличено искусственным освещением (в присутствии растений) и продуванием воды воздухом (аэрация). Обогащение кислородом путем продувания воды воздухом в аквариумах с растительностью следует проводить круглосуточно или в то время, когда аквариум лишен света. Аэрация в дневное время скорее приносит вред, чем пользу, так как создается большая, чем обычно, амплитуда колебания содержания кислорода в воде.
В практике аквариумистов дефицит кислорода обнаруживается по поведению рыб, которые в случае недостатка кислорода поднимаются в верхние слои воды и хватают воздух ртом. Мотыль, зарывшийся в песок, при недостатке кислорода выбирается из грунта и повисает на стенках аквариума; выползание малайских улиток днем из грунта также служит хорошим показателем недостатка кислорода в воде.
Такие методы контроля за содержанием кислорода в воде иногда бывают недостаточными. Для более точного определения содержания кислорода в воде можно воспользоваться химическими методами, описанными в специальных руководствах.
Углекислый газ. Углекислый газ играет очень большую роль в круговороте веществ. В воде углекислота присутствует в свободном состоянии (СО2), в соединении с водой образует угольную кислоту Н2СО3, в соединении с кальцием дает бикарбонат Са(НСО3)2 и монокарбонат СаСО3.
В свободном состоянии углекислота может растворяться в воде в весьма значительных количествах (до 2% и выше), в то время, как в воздухе содержатся обычно лишь сотые доли процента.
Углекислота образуется в результате дыхания животных и растений, за счет разложения органических веществ; при определенных условиях в воде растворяется углекислый газ воздуха.
Углерод, содержащийся в углекислоте, потребляется зелеными растениями для построения вещества клеток и тканей. В результате наблюдаются значительные суточные колебания в содержании углекислого газа в воде: днем - минимальное количество, ночью с прекращением фотосинтеза количество его увеличивается и достигает к утру максимальной величины. Особенно большие колебания происходят в аквариуме при отсутствии продувания и дополнительного освещения в зимнее вр.емя. Отрицательную роль в связи с этим играет излишнее количество растений, а летом также и «цветение» воды, т. е. развитие в ней большого количества микроскопических водорослей.
Углекислый газ, реагируя с водой, образует угольную кислоту Н2СО3, диссоциирующуюся на ионы Н+ и НСО-3. Наличие в растворе ионов водорода сдвигает активную реакцию среды в кислую сторону (в дистиллированной воде рН до 5,7):
СО2+H2О↔H2СО3↔Н++НСО-3
Стрелки указывают на то, что реакция обратима.
При полном отсутствии в воде свободного углекислого газа двууглекислые соли кальция превращаются в углекислый кальций, при этом образуются вода и углекислый газ: Ca(HCО3)2↔CaCO3+H2О + CО2.
Углекислый кальций в воде труднорастворим. Летом, обычно днем, в период наиболее энергичного фотосинтеза при интенсивном усвоении СО2 растениями растворимость СаСО3 увеличивается. Ночью вследствие дыхания животных и растений содержание СО., резко возрастает, что может привести к выпадению осадка СаСО3, который покрывает белым налетом растения к стенки аквариума,
Как уже указывалось, углекислый газ выделяется при окислении органических веществ, поэтому наличие большого количества его является в значительной степени показателем загрязнения воды аквариума. В больших концентрациях (свыше 30 мл/л) углекислый газ токсичен для рыб.
Сероводород. Сероводород в аквариуме может появится в случае недостатка кислорода (при щелочной реакции воды) и большой загрязненности. Такие условия возможны и аквариуме без искусственного продувания воды воздухом, а также в аквариуме, поставленном в темноте или лишенном растений. Сероводород может образоваться также в грунте, состоящем из очень мелкого песка.
Сероводород ядовит. Наличие его можно легко определить по запаху тухлых яиц.
Окислямость воды. Под окисляемостью понимается количество кислорода, идущее на окисление органических веществ, растворенных в 1 л воды.
В аквариуме в результате разложения избытка корма, отмерших растений и продуктов жизнедеятельности животных накапливаются органические вещества, которые, находясь на различной стадии разложения, с одной стороны, служат удобрением для растений, а с другой стороны, поглощают кислород для своего окисления. Некоторые из них оказывают ядовитое действие на рыб, затормаживают их рост и развитие, а иногда приводят к смерти. Особенно ядовиты промежуточные продукты распада, образующиеся в бескислородной среде. Различные виды рыб относятся к степени насыщенности воды органическими веществами по-разному. Обычно рыбы, живущие в мягкой кислой воде, выдерживают гораздо большие концентрации органических веществ, чем рыбы, живущие в жесткой и щелочной воде.
|
ПОИСК:
|
© Злыгостев Алексей Сергеевич, 2001-2019
При использовании материалов сайта активная ссылка обязательна:
http://aquariumlib.ru/ 'Библиотека по аквариумистике'
При использовании материалов сайта активная ссылка обязательна:
http://aquariumlib.ru/ 'Библиотека по аквариумистике'